
 |
|
|
Главная --> Справочник терминов Плотность распределена Колебания температуры плавления формовочного песка могут свидетельствовать о медленном протекании процесса отверждения, низкой прочности при растяжении и расслоении массы. Прочность массы при растяжении при комнатной температуре отражает способность формы и стержня выдерживать без повреждений те нагрузки, которые возникают при работе с этой литейной оснасткой. Прочность при растяжении при нагревании является характеристикой, указывающей на стабильность размеров формы при литье; эта характеристика сильно зависит от качества смолы. Прочностные и эксплуатационные показатели оснастки значительно повышаются при модификации новолачных смол салициловой кислотой [17] или резольными смолами. Прочность и термостойкость регулируется также количеством введенного ГМТА: увеличение его содержания до 18% (по не более) повышает плотность поперечных связей в связующем и, следовательно, его теплостойкость. Однако при высоком содержании ГМТА формы и стержни становятся более хрупкими; наилучших результатов достигают при введении 10—13% ГМТА. Молекулярный вес и поперечное сшивание. Известно, что свойства большинства полимеров зависят от изменения молекулярного веса тишь до определенной величины его. Так, сопротивление разрыву i сопротивление раздиру с увеличением молекулярного веса уве-шчиваются, а растворимость ухудшается. Полимеры для общих л,елей производят таким образом, что их молекулярный вес достигает тредела, после которого значительных изменений свойств не происходит. На этой стадии становятся важными такие показатели, как плотность поперечных сшивок и Мс. По этой причине и действительную плотность поперечных связей рассчитывают [18] согласно уравнению Портера: Переход полимера в отвержденное состояние протекает через три стадии А, В и С. В стадии А - полимер представляет собой вязкую жидкость (или твердое вещество), растворимую в воде. На стадии В - полимер является студнеобразным рыхлым телом, переходящим в дальнейшем в неплавкое и нерастворимое состояние, характерное для стадии С. В отличие от фенолоформальдегидных карбамидные полимеры даже в отвер-жденном состоянии набухают в растворителях и размягчаются при нагревании, что указывает на малое число поперечных связей, образуемых при отверждении. Увеличить плотность поперечных связей между макромолекулами в отвержденных полимерах можно введением в отверждаемую Долю структурных элементов цепи, сшитых в результате облучения дозой (г), называют плотностью поперечных связей (q). Экспериментально установлено, что плотность поперечных связей, образующихся при облучении, пропорциональна дозе и не зависит от его интенсивности Детальный механизм действия промоторов адгезии в резиновой смеси был предложен в [234]. Мета л л органические соли кобальта проявляют два независимых друг от друга эффекта: ускоряют вулканизацию и увеличивают плотность поперечных связей для резиновых смесей с высоким содержанием серы. Другое действие солей кобальта заключается в участии в реакции замещения на поверхности латуни и образовании неорганических ионов Со2+ на межфазной поверхности в процессе вулканизации. Ионы Со2+ внедряются в пленку оксида цинка при умеренных температурах перед образованием сульфидной пленки. Вероятно их присутствие в виде ионов Со3+, так как хорошо известно, что трехвалентные ионы металла в решетке оксида цинка уменьшают его удельную элект-ропро-водность и скорость диффузии ионов Zn2+ через полупроводящую пленку. При внедрении в оксид цинка перед началом сульфидирования значительного количества Со3+, образование и миграция ионов Zn2+ к поверхности замедляется. Однако диффузия включенной металлической меди к поверхности не нарушается, так как ионы Си+ мигрируют не промежуточно, а преимущественно вдоль границ зерен слоя оксида цинка [256]. Следовательно, при введении солей кобальта начальное образование сульфида цинка на поверхности корда подавляется и стимулируется быстрое образование CuxS, что видно из рисунка 20. для протекания реакции образования сульфидной пленки ZnS/ CoxSy. По мнению автора работы [234] кобальт в смеси выступает в процессе вулканизации как ингибитор всех процессов коррозии латуни, кроме коррозии её серой. Именно этим и обеспечивается устойчивость резиновых смесей, содержащих промоторы на основе кобальта, к старению в атмосфере пара. Начальная адгезия повышается вследствие того, что кобальт увеличивает плотность поперечных связей, а образующийся на поверхности раздела резина-металл сульфид кобальта имеет хорошие связующие свойства, аналогичные свойствам сульфида меди CuxS. Внедрение ионов в латунное покрытие делает его менее чувствительным к различным видам коррозии, в том числе и действию аммиака, образующегося при распаде уротропинового компонента [258]. В этом выражается синергизм действия таких систем как РУ и кобальтосодержащий промотор адгезии [259,260]. При этом кобальтосодержащие промоторы увеличивают индукционный период вулканизации, ускоряют реакцию взаимодействия серы с ускорителем и структурирование каучука. v — плотность поперечных связей. Авторы работ [133, 134] полагают, что комбинация тиазо-лового ускорителя с гидрофурамидом повышает скорость вулканизации и плотность поперечных связей в вулканизатах НК и БСК, причем синергизм этой системы объясняется повышением скорости обычно медленно протекающей реакции диссоциации комплекса на основе цинковой соли МБТ на радикалы, ном распределении по молекулярным массам плотность поперечных связей в золе qs и геле qg соответственно равны Плотность поперечных связей в серных вулканизатах НК (без ускорителя), определенная различными методами [27] •'"[ Рафиков с сотрудниками определяли методом набухания плотность поперечных связей окислительно-восстановительных полимеров на основе сшитых сополимеров стирола с дивинилбензо-лом [103], нерастворимых частей деструктированных образцов полиарилатов [94] и привитых сополимеров стирола и метилмета-крилата с янтарем [104]. В отличие от бутадиена- 1,3 в этом соединении л-электрон-ная плотность распределена неравномерно: дипольный момент винилацетилена равен 0,8 Д, причем есть основания утверждать, что отрицательным концом диполя является атом С-1, а наиболее электронодефицитным местом — атом С-4. Взаимное влияние атомов в молекуле связано, в первую очередь, с перераспределением электронной плотности в молекуле ПОД влиянием присутствующих в ней атомов или групп атомов, отличающихся по электроотрицательности. В симметричной молекуле, состоящей из схожих по электроотрицательности атомов (при условии, если молекула находится в статическом состоянии), электронная плотность распределена равномерно. Однако под влиянием реагента в органической молекуле может происходить частичное смещение электронного облака, и особенно это заметно в случае ее несимметричного строения (например, R — СН = СН2), а также, когда молекула построена из различающихся по электроотрицательности атомов. Такое смещение электронной плотности всегда происходит в сторону атома (группы) с большей электроотрицательностью: В молекуле 5Оз электронная плотность распределена таким образом, что атом серы приобретает частичный положительный заряд: между атомами углерода совершенно одинаковы, и во всех углерод-углеродных связях электронная плотность распределена равномерно: В связях С— ОН, С— СООН, С— ЫНг, С— С1, С— F электронная плотность распределена несимметрично — это так называемые по-лярные Связи. При введении в молекулу таких полярных связей (если они взаимно не компенсируются) соединение приобретает днпольный момент, В замещенных бензолах электронная плотность распределена в цикле неравномерно. Нарушение симметричности электронного облака бензольного кольца при введении в него заместителя может происходить двумя разными путями. Если заместителями являются аминогруппа, гидроксил, метоксил, метальная и тому подобные группы, которые на основании опытных данных относятся к ориентантам I рода, то электронная плотность в бензольном кольце в целом возрастает, в особенности в орто- и жг/ля-положениях по механизму р,71-сопряжения в первых двух случаях и G,TI- сопряжения (гиперконъюгация) в случае толуола: Аллил-катион также можно изобразить с помощью атомных орбиталей. Однако эта картина делокализованного катиона, в котором электронная плотность распределена по всем р-орбиталям, не дает ясного представления об отсутствии положительного заряда на центральном атоме углерода. Это обстоятельство делает метод резонансных структур более ценным *, поскольку взаимодействовать с нуклеофилом в реакциях SN1 будут только те атомы, которые несут некоторый положительный заряд. На приведенном ниже рисунке для сравнения показан локализованный катион. Реально он не существует. Это одна из резонансных структур. В отличие от бутадиена-1,3 в этом соединении л-электрон-ная плотность распределена неравномерно: диполышй момент винилацетилена равен 0,8 Д, Причем есть основания утверж дать, что отрицательным концом диполя является атом С-1, а наиболее электрон о дефицитным местом — атом С 4 В замещенных бензолах электронная плотность распределена в цикле неравномерно. Нарушение симметричности электронного облака бензольного кольца при введении в него заместителя может происходить двумя разными путями. Если заместителями являются аминогруппа, гидроксил, метоксил, метальная и тому подобные группы, которые на основании опытных данных относятся к ориентантам I рода, то электронная плотность в бензольном ядре в целом возрастает, в особенности в орто- и пара-положениях по механизму р, л-сопряжения в двух первых случаях и о, я-сопряжения (гиперконъюгация) в случае толуола: В связях С-ОН, С-СООН, С-МН2, С—Cl, C-F электронная плотность распределена несимметрично —это так называемые полярные Связи. При введении в молекулу таких полярных связей (если они взаимно не компенсируются) соединение приобретает дипольный момент. В связях С—ОН, С—СООН, С—NH», С—С1, С—F электронна' плотность распределена несимметрично —это так называемые по лярные Связи. При введении в молекулу таких полярных связе! (если они взаимно не компенсируются) соединение приобретай дипольный момент. 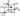 Прозрачного фильтрата Прозрачную бесцветную Пуриновых производных Пленочный испаритель Промышленное внедрение Плоскостях перпендикулярных Плоскости колебаний Плоскости симметрии Плотность дислокаций |
- |